compartilhar no whatsapp
compartilhar no telegram
compartilhar no facebook
compartilhar no linkedin
Apenas vacinas que estejam na Fase 3 de estudos clínicos no Brasil podem solicitar permissão para uso emergencial
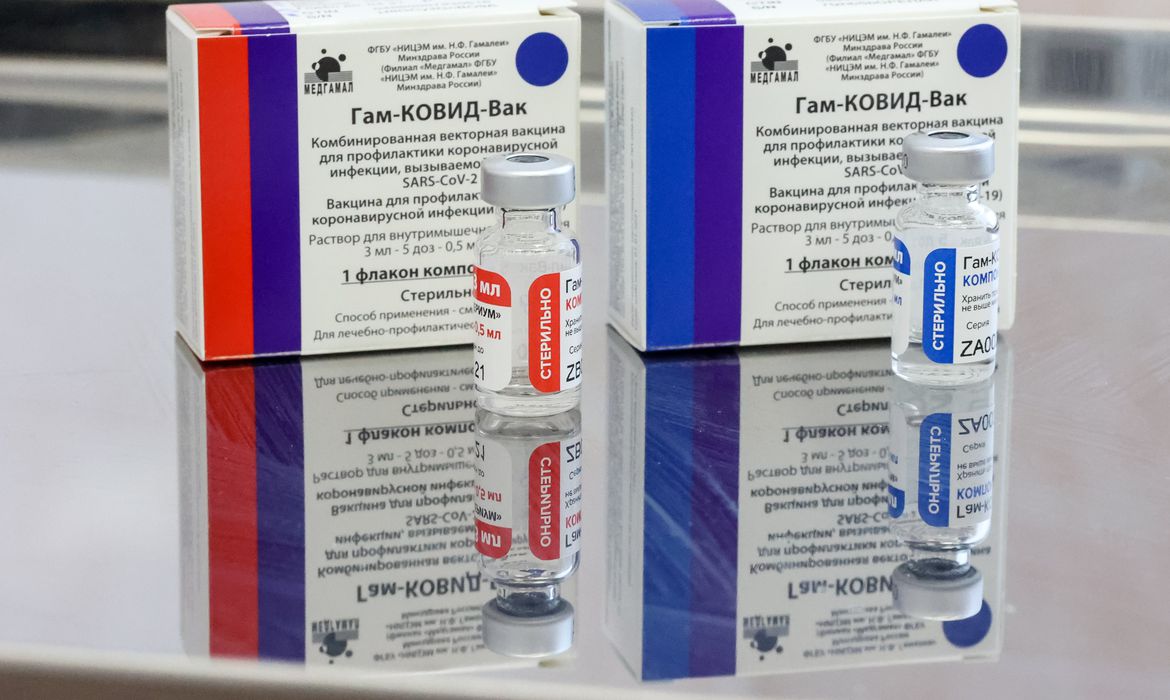 A Agência Nacional de Vigilância Sanitária (Anvisa) devolveu o pedido de uso emergencial da Sputnik V ao laboratório responsável pela vacina.
A Agência Nacional de Vigilância Sanitária (Anvisa) devolveu o pedido de uso emergencial da Sputnik V ao laboratório responsável pela vacina.
Segundo a Anvisa, o pedido foi devolvido porque o laboratório não apresentou os requisitos mínimos para que o pedido de uso emergencial pudesse ser analisado pela agência. As informações são da repórter Elaine Patrícia Cruz, da Agência Brasil.
De acordo com a Anvisa, apenas vacinas que estejam na Fase 3 de estudos clínicos no Brasil podem solicitar permissão para uso emergencial. Esse não é o caso da Sputnik V, desenvolvida pela Rússia.
A Sputnik já solicitou pedido para que os testes de Fase 3 sejam realizados no Brasil, mas isso ainda não foi aprovado pela Anvisa, já que o laboratório responsável pela vacina não enviou informações que foram solicitadas pela agência.
A autorização para as pesquisas de Fase 3 da Sputnik foi solicitada à Anvisa no dia 31 de dezembro do ano passado.
No dia 4 de janeiro deste ano, a agência constatou que faltam documentos e solicitou que o laboratório complemente as informações. A agência informou que aguarda a chegada desses dados.
 °C
°C 










 A Agência Nacional de Vigilância Sanitária (Anvisa) devolveu o pedido de uso emergencial da Sputnik V ao laboratório responsável pela vacina.
A Agência Nacional de Vigilância Sanitária (Anvisa) devolveu o pedido de uso emergencial da Sputnik V ao laboratório responsável pela vacina.