compartilhar no whatsapp
compartilhar no telegram
compartilhar no facebook
compartilhar no linkedin
Esse foi o primeiro pedido de autorização para que uma vacina contra a Covid-19 possa ser aplicada no país
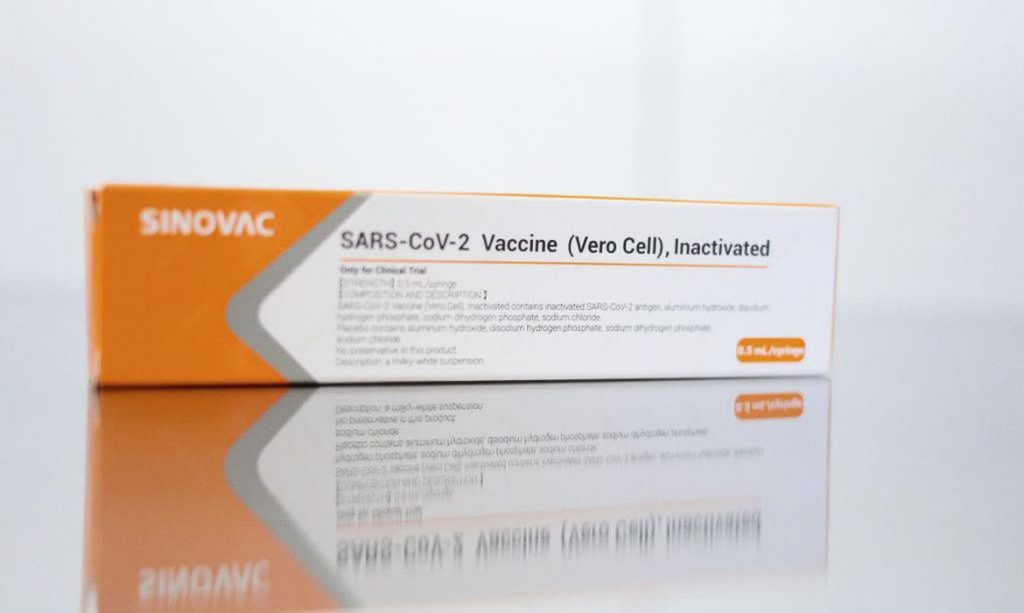
Vacina Coronavac pode sr autorizada para uso emergencial no País – Foto: Arquivo/Jornal da Franca
O Instituto Butantan pediu oficialmente à Anvisa (Agência Nacional de Vigilância Sanitária) na quinta-feira (7) autorização para uso emergencial, no Brasil, da Coronavac, nome dado à vacina contra Covid-19 desenvolvida pela empresa chinesa Sinovac e que, no Brasil, é fabricada pelo laboratório paulista.
A informação foi confirmada pela agência.
Esse é o primeiro pedido de autorização para que uma vacina contra a Covid-19 possa ser aplicada no país. Agora, a Anvisa terá dez dias para analisar os dados. As informações são da repórter Natália Cancian, da Folhapress.
Em nota, a Anvisa diz que já iniciou a triagem dos documentos presentes na solicitação e da proposta de uso emergencial.
A agência diz que pretende usar as próximas 24h para fazer uma triagem do processo e checar se todos os documentos necessários estão disponíveis.
“Se houver informação importante faltando, a Anvisa pode pausar o prazo e solicitar as informações adicionais ao laboratório”, informa.
A solicitação ocorre um dia após o instituto iniciar uma série de reuniões de pré-submissão dos dados à agência -espécie de pontapé para o pedido de aval.
Conforme antecipou o Jornal da Franca, o Butantan divulgou dados que mostram que a vacina teve eficácia de 78% nos estudos finais feitos no Brasil.
O percentual se aplica à prevenção de casos leves da doença. Casos moderados e mortes foram completamente evitados no estudo, que teve dados revisados na Áustria pelo Comitê Internacional Independente.
Embora a Anvisa dê o prazo de dez dias, a expectativa de membros do Butantan é que a análise ocorra de forma rápida, já que o instituto já compartilhava dados da vacina com a agência nos últimos meses, por meio de um processo chamado de submissão contínua.
Ainda na quinta (7), o ministro da Saúde, Eduardo Pazuello, informou que a pasta assinou um contrato com o Butantan para compra de 100 milhões de doses da Coronavac.
Segundo o ministro, o contrato prevê que as primeiras 46 milhões de doses sejam entregues até abril, e que o restante (54 milhões) seja repassado pelo instituto paulista ao governo federal no decorrer do ano.
Segundo a Anvisa, a análise do pedido de uso emergencial será feita por uma equipe multidisciplinar, que envolve especialistas de diferentes áreas.
 °C
°C